Kriget mot bakterierna
Stora spektakulära epidemier som digerdöden på 1300-talet och spanska sjukan 1918-
20 hade sannolikt kunnat undvikas om det då funnits tillgång till dagens mediciner. Men fastän det numera finns penicillin och vacciner har människan ännu inte besegrat infektionssjukdomarna. Ännu i dag orsakas vart fjärde dödsfall i världen av kända infektioner.
På senare år har även välkända bakterier med förändrade egenskaper kommit i fokus. Vi ser exempelvis att förekomsten av bakterier med motståndskraft mot antibiotika ökar där sådana läkemedel används mycket.
Dessutom växer misstankarna om att bakterier och virus kan ligga bakom uppkomsten av ett flertal stora folksjukdomar. Efter decennier av larm om cancerrisker från miljögifter, har mikroorganismernas roll bakom utvecklingen av cancer nu fått stor uppmärksamhet.
Gamla bakterier, nya egenskaper
Bakterier fanns på jordens yta i två miljarder år innan någon flercellig organism lyckades etablera sig. De har alltså haft gott om tid på sig att optimera sin förmåga att anpassa sig mot olika hot. Och för bakterier är antibiotika ett sådant hot. Deras korta generationstid gör att anpassningen kan gå fort. Därför är det inte så förvånande att många bakterieslag förvärvat motståndskraft och utvecklat resistens efter 50 år med antibiotika.Både tuberkulos och mjältbrand är sjukdomar som läkare och forskare inte trodde skulle komma tillbaka när den antibakteriella arsenalen av läkemedel ökade. Det har visat sig vara fel. I fallet tuberkulos har hiv-epidemin spelat stor roll för ökningen. Vid hiv sviktar kroppens immunförsvar. Det ger fritt spelrum för bakterier att spridas i kroppen. Dessutom har bakterier ibland förvärvad resistens mot de tidigare verksamma medlen. Det innebär att när man väl har diagnostiserat infektionen kan man inte behandla den på bästa sätt. Läkemedlen är också dyra, vilket gör tillgången begränsad i utvecklingsländerna. Allt sammantaget visar att en gammal sjukdom lätt kan komma tillbaka när förutsättningarna finns.
Mjältbrandsbakterien Bacillus anthracis, eller antrax som den populärt kallas, är inte ett hot om man ser till den naturliga smittrisken. Här har dock det senaste året visat hur människan själv kan ställa till det för sig genom att sprida bakterien på olika, raffinerade sätt.
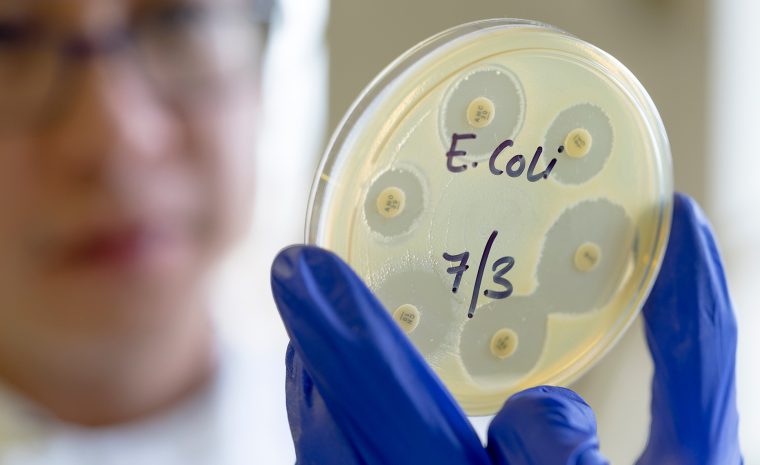
Även bakterier i vår normala tarmflora kan ändra egenskaper och bli sjukdomsframkallande. Ett aktuellt sådant exempel är ehec. Det s k ehec-syndromet innebär att patienten drabbas av blödningar och njursvikt. Sjukdomsbilden beskrevs första gången i början av 1980-talet. Det visade sig då att den vanligtvis så beskedliga tarmbakterien E coli har tagit upp främmande arvsmassa som gjort att den kan tillverka ett gift som sprids till blodet. Den blev i och med detta en sjukdomsframkallande eller s k patogen bakterie. Smittvägen är ofta livsmedel, framför allt kött.
Förra året var det tjugo år sedan den första rapporten kom som visade på sambandet mellan magsår och infektion med bakterien Helicobacter pylori (se nedre rutan på sidan 16). Fyndet revolutionerade synen på magsår och magsårsbehandling och på bakteriella infektioner. Läkarna kan nu med en veckas behandling av bakterieinfektionen bota en sjukdom som tidigare bara kunde lindras.
Bakterie gav ny syn på magsår
Infektionen är inte ny utan har troligen funnits hos både människor och djur i tusentals år. Man räknar med att hälften av jordens befolkning är infekterad, men bara en liten andel utvecklar sjukdom i mag-tarmkanalen. Då uppkommer frågan om det är rätt att behandla alla infekterade och vad detta i så fall kostar samhället och individen. Självklart ska patienter med magsår och H pylori-infektion behandlas. Problemen uppstår eftersom det inte går att förutsäga vilka av de infekterade personerna som senare i livet utvecklar sår eller cancer i magsäcken till följd av en ständigt pågående infektion med bakterien. Här måste man väga in risken för att det sker en urvalsprocess som gynnar just motståndskraftiga eller resistenta bakterier.En annan bakterie som verkar ligga bakom en folksjukdom är en ny art av bakteriesläktet klamydia. Arten beskrevs första gången i mitten av 1980-talet och fick populärt namnet twar. Dess riktiga namn, Chlamydia pneumoniae, ger en fingervisning om var den naturligt infekterar kroppen: i lungorna. Bakterien är mycket svår att odla (liksom magsårsbakterien H pylori), och detta kan förklara varför den inte gick att koppla ihop med lunginflammation tidigare. I dag spekuleras det över samband mellan denna klamydiaart och hjärt-kärlsjukdom. Även orienterardöden och plötslig hjärtdöd kopplades i början till twar-infektion.
Sambandet mellan hjärt-kärlsjukdom och C pneumoniae är dock inte lika klart som mellan H pylori och magsår. Många studier pågår där man provar att behandla hjärtsjuka patientgrupper med antibiotika och sedan jämför dem med obehandlade kontrollgrupper. Svaren dröjer, och ännu är det för tidigt att gå ut med en allmän rekommendation att behandla hjärtpatienter med antibiotika. Samma resonemang som vid H pylori-infektion och risken att utveckla resistens måste gälla även här.
Campylobacter, legionella och bartonella är tre exempel på nya bakteriearter som upptäckts de senaste 25 åren. Campylobacter ligger bakom den i dag vanligaste rapporterade bakteriella diarrésjukdomen i Sverige med ca 8 000 fall förra året.
Legionella är fruktad hos individer med nedsatt immunförsvar eftersom den ger upphov till bl a lunginflammation. Den sprids med vatten som inte upphettats tillräckligt och har orsakat ett flertal allvarliga utbrott på svenska sjukhus under 1990-talet.
Bartonella orsakar den s k kattklössjukan och upptäcktes med DNA-teknik för ca tio år sedan. Med hjälp av den kunskap som sådana test gav kunde man sedan odla bakterien i laboratorium. Detta är nödvändigt för att kunna studera den noggrant. Med nya DNA-baserade tekniker kommer forskarna säkert att finna ännu fler arter som kan kopplas till sjukdomar där den utlösande orsaken är okänd i dag.
Är alla sjukdomar infektioner?
Många sjukdomar uppträder som en infektionssjukdom vad gäller spridning och anhopning under en viss tid. Det antyder att sjukdomen kan vara orsakad av bakterier eller virus.I den medicinska litteraturen kommer också nästan dagligen uppgifter om nya samband mellan sjukdom och mikroorganismer. Det har rapporterats om samband mellan H pylori och plötslig spädbarnsdöd, mellan diverse hudsjukdomar och hjärt-kärlsjukdom, mellan s k nanobakterier och njursten, mellan olika virus och tumörsjukdomar och mellan mykobakterier och inflammatorisk tarmsjukdom – listan kan göras längre. Men i de allra flesta fall rör det sig om samband som inte synts vid nya och mer välgjorda studier. Ett problem är att många observationer bygger på ett fåtal fall där man möjligen skulle kunna ana en koppling.
I fallet H pylori och magsår tog det över tio år och flera väl underbyggda studier där sambandet kunde fastställas innan de kliniskt verksamma läkarna var övertygade.
Kronisk inflammation bra?
De flesta anser nog att en inflammation är något dåligt för kroppen. Men man skulle kunna vända på resonemanget och se inflammationen som en positiv reaktion för att få bort den skadliga bakterien. Problemet är dock när kroppen inte kan göra sig kvitt mikroorganismen. Inflammationen pågår då ständigt och blir kronisk. I fallet gastrit eller inflammation i magslemhinnan har en del forskare argumenterat för att även detta tillstånd skulle vara bra för vår beredskap mot främmande mikroorganismer. Om en bakterie stimulerar inflammationen så är kroppen så att säga beredd att försvara sig när andra aggressiva bakterier dyker upp. Det fungerar som ett slags naturlig vaccination. I så fall skulle kanske H pylori räknas till normalfloran (se övre rutan på sidan 16).Resistenta bakterier
Själva fenomenet att bakterier kan ta upp DNA från sin omgivning och på så sätt omvandlas till aggressiva bakterier har visat sig vara vanligt. Det är bl a denna förmåga som ligger bakom att bakterier kan bli motståndskraftiga mot antibiotika. Nyligen genomförda studier i Sverige och andra länder har presenterat en ny förklaringsmodell till hur resistenta bakterier sprids.Tidigare trodde forskarna att bakterier i och med sina förändrade egenskaper i arvsmassan även förlorar i överlevnadsförmåga. Det skulle således kosta något för bakterien att bli resistent. Och det i sin tur medför att denna resistenta population i längden försvinner i konkurrens med starkare bakterier utan resistensgener. När detta studeras i provrör verkar hypotesen stämma. Men i verkligheten ser det annorlunda ut. Det har visat sig att resistenta bakterier som infekterar ett djur eller en människa kan kompensera genom att förändra sin arvsmassa i vissa delar. De återtar då sin överlevnadsförmåga och kan till och med konkurrera ut andra bakterier.
Detta scenario kan i verkligheten innebära att sådana bakterier lätt kan sprida sig pga sin förbättrade överlevnadsförmåga. De sprider då samtidigt antibiotikaresistensen i befolkningen. Vi har sett detta när det gäller vissa streptokocksjukdomar och tuberkulos. Och om det inträffar hos exempelvis sjukhussjukebakterien MRSA eller vid spridning av tuberkulos kan situationen bli ytterst besvärlig.
De nya DNA-teknikerna genererar mycket ny information. Nya forskningsområden växer upp varav bioinformatik är ett. I dag används informationen mest i forskningsprojekt. Men inom några år kommer datakraft och expertis att finnas tillgängliga även ute på vårdcentralerna via nätverk och Internetuppkoppling.
Bättre behandling om tio år
En framtidsbild skulle kunna vara att läkaren tar ett blodprov och ett prov från själva infektionshärden. Blodprovet analyseras med DNA-teknik och sedan skickas denna information till analyscentralen. Vi får då uppgift om hur patientens arvsmassa ser ut.Från infektionsprovet erhålls information om den aktuella mikroorganismen – om den är känslig för antibiotika eller om den innehåller specifika virulensgener som gör den motståndskraftig. Allt sammantaget kan ge en bättre bedömning av den enskilde patienten och då även styra behandlingen.
Vi skulle då exempelvis kunna fånga upp de individer som löper risk att bli allvarligt sjuka av den s k mördarbakterien Streptococcus pyogenes och behandla dessa. De flesta människor riskerar bara en vanlig halsfluss och klarar sig utan behandling. Men vissa är mer känsliga och måste därför få antibiotika. Tidigare har alla behandlats säkerhets skull. Men med tillgång till information om hur känslig just den sökande patienten är, kan läkaren ta beslutet att inte behandla med antibiotika. Då går det dessutom att minska förskrivningen av antibiotika.
Normalfloran är bra för oss
Det är viktigt att komma ihåg att inte alla bakterier är skadliga för oss. Exempelvis är bakterierna i vår normalflora ofarliga och nödvändiga för vår existens. Vi har tio gånger fler bakterieceller i kroppen än egna kroppsceller, främst i tarmarna.
Vissa bakterier kan vi tillsätta maten för att på så sätt ”förbättra” vår normalflora. Hit hör exempelvis lactobaciller (bilden). Fler och fler börjar intressera sig för en alternativ väg att bekämpa de sjukdomsframkallande bakterierna. Alternativet benämns på engelska probiotics. Det innebär att snälla bakterier ersätter de sjukdomsframkallande bakterierna eller kanske tonar ner ett alltför kraftigt och därmed skadligt immunsvar på platsen för infektionen.
Bakterier kan också göra nytta genom att minska allergirisken. Man har bl a visat att ju fler bakterier från normalfloran som en nyfödd får i sig under de första månaderna, desto mindre är risken för att barnet senare utvecklar allergi (se Allergier – den goda hygienens baksida? F&F 6/02). Inom detta område pågår mycket forskning, och flera av de stora forskningsfinansiärerna stöder forskning om normalfloran och hur exempelvis antibiotika påverkar denna.
Bakterie gav ny kunskap
Första rapporten om att bakterien Helicobacter pylori orsakar magsår kom år 1982. Ungefär var tredje medelålders person i Sverige har bakterien i magsäcken och man beräknar att ca 70 procent av alla fall av magsäckscancer kan kopplas till infektion med H pylori.
Vi vet inte hur bakterien orsakar magcancer. Infektionen gör att antalet syraproducerande celler i magsäcken minskar. Men frågan är om detta i sig kan leda till tumörer. Minskad syraproduktion gör att fler bakterier kan bosätta sig i magen, och de kanske i sin tur påverkar cellerna så att de omvandlas till tumörceller.
Upptäckten av bakterien har till dags dato genererat tusentals forskarrapporter. Tack vare H pylori vet vi i dag mer om hur immunsystemet fungerar i mage och tarm. Denna kunskap kan användas vid exempelvis vaccinframställning mot andra infektioner.