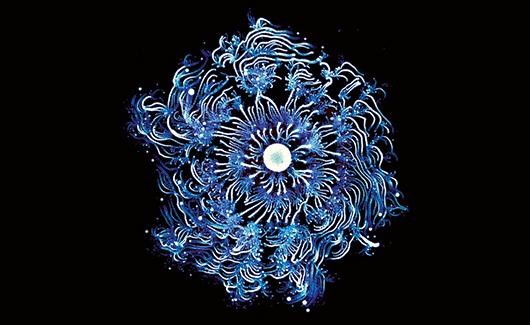
En bakteriekoloni av Paenibacillus vortex har byggt en spiral. Forskaren Eshel Ben-Jacob styr hur de ska växa genom att rista in spår på ytan och utsätta dem för olika utmaningar. Genom att manipulera sina bakteriekolonier och göra konst av dem lär han sig hur bakterierna samarbetar.
Image: Eshel Ben-Jacob
Konsten att förstå bakteriernas språk
Bakterier som kapslar in sig tillsammans i en så kallad biofilm blir nästan osårbara för vårt immunförsvar och för antibiotika. Problemet växer i takt med att fler personer behandlas med implantat. Lösningen kan vara ett ämne i vitlök, som stör bakteriernas samarbete.
Bakterier är sociala varelser som jagar i flock. Tillsammans fattar de beslut om när de ska agera, och de bygger ointagliga försvarsanläggningar i våra kroppar. Resistenta bakterier breder ut sig över hela världen och ingen ny typ av antibiotikum har lanserats på 20 år.
Att störa bakteriernas sociala gemenskap skulle kunna bota människor som drabbats av en typ av infektion som är extremt svår att få bukt med. Det handlar om infektioner som sätter sig på implantat i kroppen, till exempel hjärtklaffar och höftproteser.
Infektioner av den typen kan vara svåra att upptäcka eftersom de till en början inte gör så mycket väsen av sig. De kan utvecklas till ett livslångt lidande och kostar mycket pengar för sjukvården. Av alla nya proteser och implantat som sätts in idag, drabbas ungefär två procent av protesinfektion.
Men hur kommer det sig att bakterier sätter sig på konstgjorda implantat, och varför är de så svåra att mota bort? Jo, det beror på en förmåga som det första livet på jorden utvecklade för miljarder år sedan.
Bakterier tillverkar och nästlar in sig i ett slags slem som breder ut sig i en tunn hinna, en biofilm. De encelliga bakterierna i biofilmen agerar gemensamt som om de vore en stor flercellig organism. Ett av de allra första tecken på liv som har hittats på jorden är fossil av bakterietillverkad biofilm. Det är 3,5 miljarder år gammalt. Modern mänsklig teknologi försöker hävda sig mot en uråldrig konstruktion. Än så länge är vi chanslösa.
En övervägande del av alla bakterier på jorden lever i olika typer av biofilm. Ändå har gängse antibiotika riktat in sig på att döda de bakterier som befinner sig i fritt tillstånd och inte alls har fysisk kontakt i form av biofilm. Sedan 1980-talet har forskarna konstaterat att många infektioner orsakas av biofilmsbildande bakterier. Karies i tänderna orsakas av biofilm, till exempel. I den svåra lungsjukdomen cystisk fibros bygger Pseudomonas aeruginosa biofilm, och även i en tuberkulös lunga breder biofilm ut sig. Framför allt: ju fler främmande material vi opererar in i våra kroppar, desto fler nya ytor får bakteriefilmsbyggande bakterier att kolonisera. Till saken hör att vi också ger bakterierna bäst möjligheter att ta för sig när vi är som svagast – när vi ligger på sjukhus.
– Efter en tid på en intensivvårdsavdelning har du fått en ny bakterieflora i lungorna, och efter ytterligare en tid på vårdavdelning har magens bakterieflora förändrats, säger Anna Holmberg, som är infektionsläkare på Skånes universitetssjukhus i Lund och forskar om biofilmsrelaterade protesinfektioner.
I varje människa finns tio gånger fler bakterier än egna celler. En del bakterier är fruktade, men de flesta är alldeles nödvändiga, hårt arbetande encelliga organismer, som lever på vår hud och i våra magar, tar hand om näring och tränar vårt immunsystem. Därför är det viktigt att vi håller sams med dem. Men 70 års användning av antibiotika har fått balansen att rubbas. Vårt framgångsrika krig mot sjukdomsalstrande bakterier har förmått snälla bakterier att mutera och bli resistenta. Naturligt förekommande hudbakterier och tarmbakterier som enterokocker har vänt sig emot oss. De tar sig till ställen i kroppen där de inte ska vara, och där blir de skadliga. Vid operationer får de möjlighet att fästa vid proteserna. Och när biofilmen väl har fastnat sitter den hårt.
– Biofilmen är som en fritidsgård för bakterier, där enterokocker och stafylokocker byter resistenta gener med varandra. Bakterierna är tusen gånger mer resistenta i biofilmen än utanför, säger Anna Holmberg.
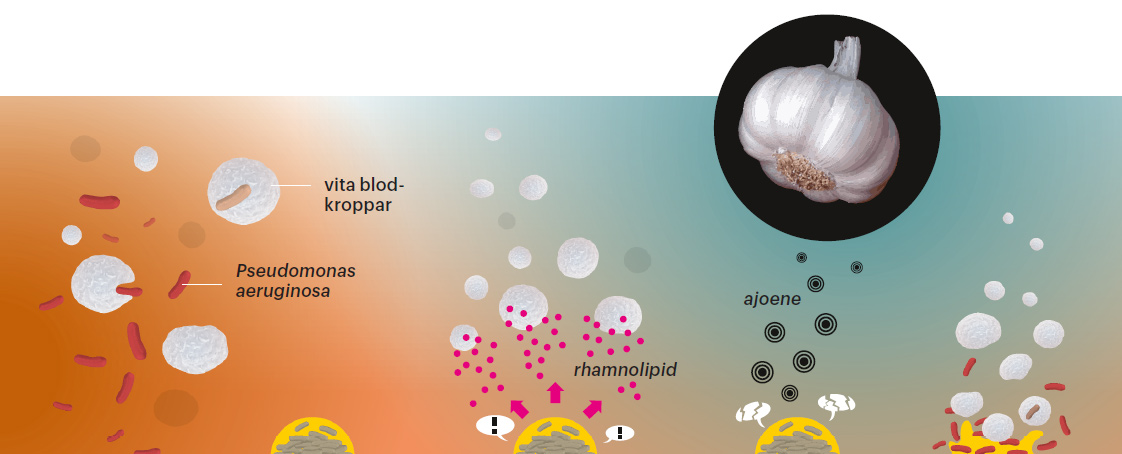
1. I fritt simmande tillstånd är bakterien Pseudomonas aeruginosa sårbar för attacker från immunförsvarets vita blodkroppar och antibiotika.
2. När bakterierna fäster mot en yta och tillsammans bildar en så kallad biofilm blir de tusen gånger mer motståndskraftiga än i fritt tillstånd.
3. För att ytterligare öka sitt försvar kommunicerar bakterierna med varandra och kommer överens om att tillverka ett ämne, rhamnolipid, som angriper de vita blodkropparna.
4. En substans i vitlök, ajoene, har visat sig störa ut bakteriernas kommunikation, så att de tappar förmågan att producera rhamnolipid.
5. När kommunikationsförmågan är utslagen försvagas bakteriernas försvar mot de vita blodkropparna, som nu kan invadera biofilmen.
Bild: Johan Jarnestad
Bakterierna som befinner sig i biofilmens yttersta skikt skyddar dem som ligger innanför. Ytterskiktet är mest utsatt för immunförsvarets attacker och för antibiotika. Men bakterierna där har också direktkontakt med blodet där deras näring finns, som gör att de kan föröka sig snabbt. Biofilmens intimitet gör att bakterierna ligger tätt intill varandra och lätt kan utbyta gener och på så sätt utveckla resistens. Längst in i biofilmen råder syrebrist och där gömmer sig de mest förrädiska, de som har dragit ner på sin ämnesomsättning för att uthärda. Man kan säga att de sover, och de vita blodkropparna, som ska bekämpa dem, märker dem inte. Om biofilmen avlägsnas men några få sådana bakterier blir kvar, så kan de vakna, börja dela sig och starta en helt ny koloni. Därför är det viktigt att allt främmande material runt en protes plockas bort när infektionen ska övervinnas, alltså inte bara själva protesen, utan också skruvar och bencement.
Biofilmerna är förrädiska, men de kan också vara vackra. Den israeliske fysikern Eshel Ben-Jacob odlar bakterier och utsätter dem för utmaningar som näringsbrist och olidliga temperaturer. Bakterierna agerar i grupp och sätts i rörelse i hans petriskålar. Han färgsätter dem, och fram kommer psykedeliska mönster att förundras över. Filmerna är som konstverk, men det finns också ett vetenskapligt syfte med studierna. Bakteriefilmens utseende skulle kunna avslöja mekanismerna bakom bakteriernas gemensamma skydd, och förstår vi dessa skulle vi också kunna rasera skyddet.
– Vi odlar också vackra biofilmer, säger Ute Römling, som är cellbiolog på Karolinska institutet och visar upp en bild på en rödfärgad koloni av Salmonella typhimurium.
Färgen binder till det material som bakterierna utsöndrar, och därför blir biofilmen röd. Materialet kallas för matrix, och är den sega biofilm som skyddar bakterierna. Tjocka röda ådror vecklar ut sig och mynnar ut i tunnare trådar. Matrixen består av ett både hårt och segt material som klistrar ihop bakterierna med varandra och med den yta som den har fastnat på.
– Förut kallades biofilm för bakterievirke, bacterial wood, och nu vet vi att den består av cellulosa och ett protein av klassen amyloid – samma slags hårda plack som sprider sig i hjärnan hos alzheimersjuka. Om man tar tag i biofilmen med en pincett är det som att ta tag i tuggummi.
Det var Ute Römling som gjorde den genetiska och kemiska analysen och insåg att biofilm består av cellulosa. Hon och hennes forskargrupp kom på hur bakterierna bar sig åt för att skapa den.
Fram till 1980-talet var det ingen som trodde att sjukdomsalstrande bakterier ägnade sig åt att bygga biofilm. Sedan upptäckte man att Pseudomonas aeruginosa kapslar in sig i biofilm vid cystisk fibros. År 1998 publicerade Science en mycket betydelsefull artikel där forskarna konstaterade att biofilmsbildande bakterier ligger bakom många kroniska infektioner. Frågan var bara hur de bar sig åt för att bygga så slitstarka försvarsanläggningar.
– Det märkliga var att bakterier av släktena Salmonella och Pseudomonas och arten Escherichia-coli skapar biofilmer som ser likadana ut. Vi ansåg att det borde betyda att samma princip styrde biofilmstillverkningen för de flesta bakterier, säger Ute Römling.
Hon fann ett styrsystem hos bakterierna som styr över biofilmstillverkningen. Ett ämne som de kallar för cykliskt di-GMP bestämmer när en bakterie ska börja tillverka den sega biofilmen, och när den ska släppa taget och simma i väg. Är cykliskt di-GMP-nivån hög hos en bakterie producerar den mycket biofilm, och sjunker nivåerna så släpper bakterierna taget om varandra.
Kroppen har många egna försvarssystem mot biofilm; de bildas naturligt i bland annat tarmen. Det pågår ett lågintensivt krig där antibakteriella peptider bidrar med att hålla biofilmen i schack. Ute Römling tror på behandling mot biofilmsinfektioner som innebär en kombination av nedbrytande peptider och antibiotika. Tanken är att dessa tillsammans ska bekämpa biofilm som börjat gro på platser där den inte bör finnas.
Bakteriernas urgamla förmåga att bygga egna försvarsborgar har att göra med deras sinnrika förmåga att samordna sina attacker. Länge ansågs bakterier vara encelliga nomader som enbart reagerade på sin närmaste omgivning. En bakteries högsta önskan var att bli två bakterier. Alltså äta, dela på sig och sedan dö. Paradigmskiftet i synen på bakteriernas liv har skett mycket tack vare forskare som Peter Greenberg. Han kallar sig sociomikrobiolog och är verksam vid University of Washington i Seattle, USA.
– Man trodde inte att bakterierna hade någon användning av att vara sociala. Nu vet vi att de både samarbetar och har konflikter. Är inte det att vara social? säger han.
Peter Greenberg var också med och namngav bakteriernas sociala förmåga: quorum sensing. En liten bakterie kan på egen hand inte göra en fluga förnär, men när den tillsammans synkroniserar attackerna blir den desto starkare. Quorum är en juridisk term som kommer från latinet och står för det antal som måste vara närvarande vid ett möte för att beslut ska kunna fattas. På samma sätt ”folkomröstar” bakterier. De räknar in varandra för att de ska vara tillräckligt starka för att kunna agera effektivt. I grupp beter de sig som en stor flercellig organism, men utan gemensam hjärna.
Det var en liten självlysande bläckfisk på Hawaii som fångade Peter Greenbergs intresse och som skulle avslöja bakteriernas sociala liv.
När biofilmen blir farlig
Kvinna 45 år som i sex år levt med en kronisk obotlig infektion i sin höftledsprotes. Infektionen gav sig till känna två år efter att protesen satts in. En böld växte till på utsidan av höften, sprack och blev ett svårläkt och ymnigt vätskande sår. Till en början var det problem att ens kunna urskilja några bakterier som orsakade infektionen, men efter hand har det konstaterats att tre olika typer av bakterier, en vit stafylokock, en hud- och en tarmbakterie, har fäst sig på hennes höftprotes, och det finns inget som kan få dem att vika undan. Det finns ett botemedel, och det är att helt sonika avlägsna allt främmande material och efter en tid sätta in en helt ny protes. I just det här fallet är detta dock inte möjligt, och därför måste kvinnan leva med att infektionen med jämna mellanrum blossar upp och orsakar vätskande sår som måste läggas om dagligen.
När månen lyser över de grunda stränderna på Hawaii är smådjuren lättfångade byten. Men den lilla bläckfisken Euprymna scolopes har ett samarbete med den självlysande bakterien Vibrio fischeri, vilket skyddar den från rovdjurens käftar. Livet är farligt för små nattlevande djur i de här grunda vattnen. Månljuset bildar skuggor av dem på botten, och ett rovdjur som befinner sig i den skuggan vet att rakt ovanför simmar nattens middag. Men Euprymna scolopes kamouflerar sig genom att liksom tända en lampa, lika stark som månens ljus, ner mot havsbotten. Lampan som tänds är en koloni av Vibrio fischeri, som bor i bläckfiskens kropp. Bakterierna känner av hur starkt månskenet är. De samordnar sig och lyser precis så starkt som behövs för att trolla bort bläckfiskens skugga på sandbotten. Resultatet är att bläckfisken blir osynlig för de hungriga rovdjuren.
När gryningen kommer kryper bläckfisken ner i sanden och tömmer hela sin reserv av förbrukade bakterier. Under dagen växer nya ljusalstrande bakterier till inför nästa natts utmaning i månskenet.
Peter Greenberg bekantade sig med den här märkliga bläckfisken när han var forskarstudent i början av 1970-talet. Av en slump kom han att lyssna på en föreläsning av myrforskaren Edward Wilson, som lanserade sociobiologi, en vetenskap om de sociala beteendenas evolutionära grund.
– Efter Edward Wilsons föreläsning slog det mig att bakterierna kanske också var sociala och att de kommunicerade med ett kemiskt ämne för att avgöra när det var dags att lysa. Det var inte så många som trodde på det, men jag bestämde mig för att det var det här jag skulle forska om.
Det tog några år, men Peter Greenberg listade ut att de marina bioluminiscenta bakterierna, som alltså sänder ut ljus, faktiskt kommunicerade, och hur de gjorde det. Han fann att de skickar kemiska signaler till varandra, och han identifierade de gener som är aktiva i den processen. Bakterierna räknar in varandra genom att släppa ut en molekyl, en quorum sensing-signal, som säger ”Här är jag”. Och samtidigt kan de läsa av andras ”Jag är också här”. På så sätt får de veta att de är tillräckligt många för att bläckfisken ska lysa så starkt som det krävs för att dölja sin egen skugga. Ljusskenet från en ensam liten bakterie går knappt att urskilja och ensam skulle den bara slösa energi till ingen nytta. Vibrio fischeri tjänar alltså sitt uppehälle och får njuta av lyxen att bo hos bläckfisken genom att gemensamt fatta beslut om när det är dags att tända lamporna.
– De flesta biologer antog att det här var en unik företeelse som bara bioluminiscenta bakterier ägnar sig åt, och att det inte alls var vanligt att andra typer av bakterier synkroniserar sig på det viset. Jag tänkte att alla bakterier hade den förmågan, men kunde först inte bevisa det, säger Peter Greenberg.
Peter Greenberg misstänkte att Vibrio fischeri hade avslöjat en fundamental egenskap hos alla typer av bakterier. Deras självlysande förmåga hade gjort dem enkla för honom att upptäcka och undersöka. Nu gällde det att visa att även andra typer av bakterier gillar att svärma och samordna sina aktiviteter, som att släppa ut gifter, bygga skyddande biofilm och attackera immunförsvarets vita blodkroppar.
Så, i början av 1990-talet brakade det loss, mycket tack vare att tekniken att sekvensera dna, det vill säga läsa av arvsmassan, började användas på bred front. Flera forskarlag identifierade gener som var kopplade till tillverkning av quorum sensing-signaler, även hos sjukdomsframkallande bakterier som Pseudomonas aeruginosa. Denna trivs vanligtvis i vattendrag och jord, men orsakar också urinvägsinfektioner, lunginflammationer, sår-, hud- och ögoninfektioner. Bakterierna av släktet Pseudomonas är också skyldiga till lunginfektionen hos dem som är drabbade av cystisk fibros och slår hårt mot dem som redan är svaga av sjukdom och därför har ett nedsatt immunförsvar. Så när det gick upp för forskarvärlden att även sjukdomsbringande bakterier har förmågan att samordna sina giftiga attacker blev det här ett stort och viktigt forskningsområde.
En annan pionjär på området, Bonnie Bassler, professor i mikrobiologi vid Princeton university i USA, kunde i mitten av 1990-talet visa att bakterier inte bara talar med sina artfränder, utan också kan sända och ta emot signaler från andra arter. Bakteriernas kolonier är mångkulturella samhällen där olika arter både samsas och strider om resurserna.
– Biofilm kan också bildas utan att bakterierna kommunicerar – men sådan biofilm ser helt onormal ut. Quorum sensing styr på något sätt biofilmens utseende, säger Peter Greenberg.
Och det är de här signalerna forskarna vill tjuvlyssna på och blockera. I Köpenhamn har lyckade försök gjorts med – vitlök.
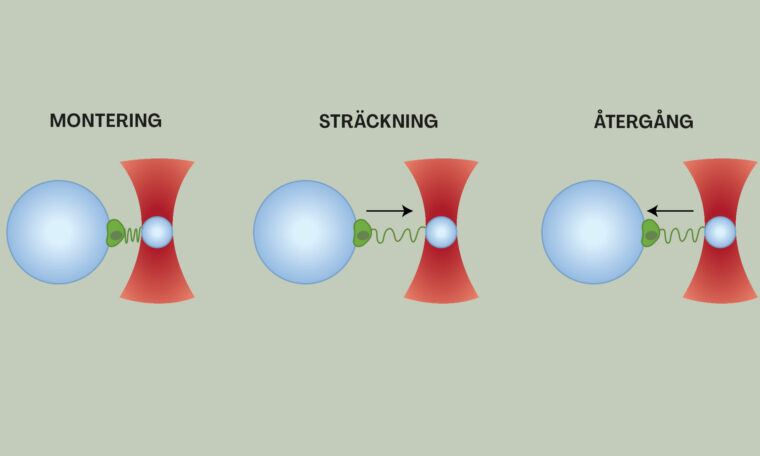
Mikrobiologen Tim Holm Jakobsen och hans kolleger har lyckats bota försöksmöss som drabbats av en biofilmsinfektion på en inopererad plastbit, som var infekterad med Pseudomonas aeruginosa. Försöket gick ut på att undersöka om det gick att bryta ner biofilmen genom att tillföra ett ämne, ajoene, extraherat ur vitlök.
– Ajoene dödar inte bakterierna, men det blockerade quorum sensing-systemet så att bakterierna inte kunde kommunicera, säger Tim Holm Jakobsen.
Utan kommunikation kan bakterierna inte samordna sina attacker mot immunförsvarets vita blodkroppar, men de är fortfarande giftiga och sjukdomsframkallande. Ett starkt och friskt immunförsvar kan räcka för att ta hand om de vapenlösa bakterierna, annars behövs dessvärre en dos antibiotika för att göra resten av jobbet.
– Vi plockade ut plastbiten och kunde konstatera att vi verkligen hade lyckats lösa upp den hårda biofilmen.
Nu väntar Tim Holm Jakobsen på att ett läkemedelsföretag ska köpa patentet, så att stora kliniska prövningar kan genomföras.

Fördelen med att bota infektioner genom att slå ut quorum sensing-systemet är att det inte provocerar fram ett försvar hos bakterierna som får dem att mutera och bli resistenta. Det fungerar också på bakterier som är helt motståndskraftiga mot konventionell antibiotikabehandling, vare sig de befinner sig i en biofilm eller är fritt simmande nomader.
Många letar i dag efter quorum sensing-störande substanser i växter. Vitlök är sedan länge känd för att vara antibakteriell, och kanske är det just dess förmåga att störa kommunikationen mellan bakterierna som gör den så effektiv. Ginseng har också visat sig ha vissa quorum sensing-störande egenskaper, men ännu har ingen lyckats urskilja dess verksamma substans.
Peter Greenberg, som har ägnat hela sin forskarkarriär åt kommunicerande och biofilmsbyggande bakterier, tycker att forskningen i Köpenhamn är en av de allra mest lovande just nu. Han menar dock att man ännu är långt från att förstå hur bakterierna kommunicerar med varandra i biofilm. Själv letar han efter quorum sensing-systemets akilleshäl, där kommunikationen är som viktigast för bakteriekolonins överlevnad. Och precis där vill han slå till.
Peter Greenberg har lyckats utnyttja muterade gratisätare i sina experiment. Det är bakterier som uppstår naturligt i en långvarig infektion och tar för sig av näring, utan att arbeta för sig. I vanlig biofilm, liksom i ett samhälle, accepteras en begränsad mängd gratisätare. Men blir de för många rasar hela samhällsstrukturen.
Han odlade Pseudomonas aeruginosa i en månad och använde proteiner som energikälla för dem. Bakterierna behöver kommunicera för att gemensamt bryta ner proteinet, tillgodogöra sig näringen och växa. Peter Greenberg hade tagit bort ammoniaken, som Pseudomonas gillar, eftersom den innehåller kväve. På så sätt tvingade han bakterierna att arbeta hårdare för att lyckas utvinna tillräckliga mängder med kväve ur proteinet som stod till buds. Priset för maten blev helt enkelt väldigt högt! Det innebar att det blev en ännu större vinst för en bakterie att muteras till gratisätare och fritt ta för sig av de andra, hårt arbetande, bakteriernas nedbrytningsprodukter. Följden blev att allt fler muterade till gratisätare. De tog över – helt plötsligt fanns det inte tillräckligt många som kunde bryta ner näringen och hela populationen kollapsade.
Så Peter Greenbergs dröm är att helt enkelt lura de sociala bakterierna genom att göra arbetsinsatsen så hög att de hellre börjar snylta. Antibiotika – som de fungerar i dag –tvingar bakterierna att mutera och bli resistenta. Den här metoden tvingar dem i stället att mutera till gratisätare. En sådan koloni kan inte bestå, den dör av näringsbrist. Men att provocera fram gratisätande bakterier i svåra infektioner är långt ifrån verklighet i dag, och Peter Greenberg vet inte heller hur det praktiskt skulle gå till.
– Jag kallar det för min pie in the sky. Det är ett uttryck vi amerikaner använder när vi pratar om våra drömmar. Det finns inga pajer i himlen, men tänk om det ändå gjorde det.