Förhoppningar om framtida bot
En tanke inom nanomedicinen är att man genom att använda partiklar ska kunna koppla ihop flera funktioner. Medan en läkemedelsmolekyl oftast bara gör en enda sak, skulle en nanopartikel exempelvis både kunna hitta till tumören, göra den synlig och oskadliggöra den.
Nanoelektroder avläser hjärnan
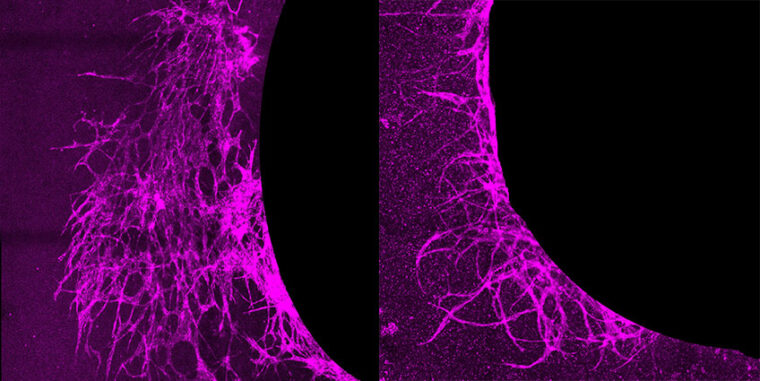
Neurofysiologen Jens Schouenborg leder arbetet vid det nystartade Neuronanoscience Research Center i Lund. Här vill man skapa nanoelektroder som ska kunna implanteras i hjärnan och båda läsa och sända signaler. Med hjälp av signalerna hoppas forskarna kunna studera grundläggande inlärnings- och minnesmekanismer.
En framtida klinisk tillämpning är att bättre kunna behandla parkinsonpatienter med djupstimulering. Sådan görs redan i dag, men elektroderna är mycket grova. En annan förhoppning är att kunna stimulera hjärnan för att släcka ut smärtimpulser hos personer med kroniska smärttillstånd.
– Detta prövades under 1970- och 80-talen, men problemet var att elektroderna rörde sig. I hjärnan ligger olika centra tätt, så patienten kunde då råka ut för att drabbas av panik i stället för att få smärtlindring. Den nya typen av elektroder skulle vara mycket mindre och gå att fästa i vävnaden så de inte rör sig, förklarar Jens Schouenborg.
Men tillämpningarna ligger 5-10 år framåt. Först måste man konstruera elektroderna, se att de har tillräckligt bra ledningsförmåga och förvissa sig om att de inte är skadliga.
Botar blindhet och stämmer blod
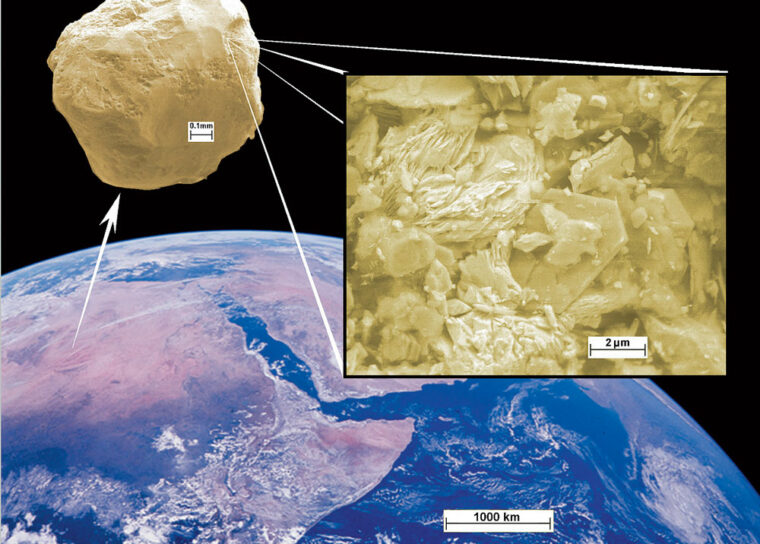
Den amerikanske forskaren Rutledge Ellis-Behnkes grupp vid Massachusetts Institute of Technology väckte stor uppmärksamhet i somras. Då presenterade de hur de genom att spruta in nanopartiklar i hjärnan på hamstrar som gjorts blinda kunde ge djuren synen tillbaka.
Hamstrarnas synbortfall berodde på att synnerven skurits av. Men när de nanometerlånga peptiderna, det vill säga korta kedjor av aminosyror, kom in i hjärnan började nervcellerna läka ihop.
Nyligen visade forskargruppen att en annan peptid sekundsnabbt kan stoppa blödning i flera olika vävnader hos försöksdjur, som levern, huden, ryggmärgen, hjärnan och inälvorna. Detta skulle kunna göra att operationer kan utföras snabbare och säkrare. Minskat blodflöde gör det lättare för kirurgen att se vad hon eller han gör.
Kväver och kokar tumörer
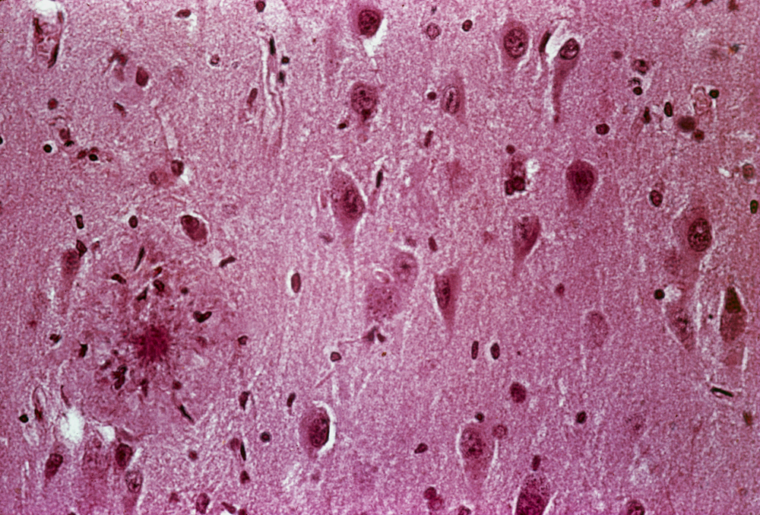
Nyligen presenterade professor Erkki Ruoslahti vid Burnham Institute for Medical Research i Kalifornien speciella peptider som hittar till blodkärl i tumörer. I tumörer finns mycket levrat blod i kärlväggarna, något som är ovanligt i friska blodkärl. När forskarna kopplade den målsökande peptiden till nanostora partiklar av järnoxid (som normalt används vid magnetresonansavbildning) gick det att se var tumören var belägen.
Partiklarna visade sig också likna levrat blod i så måtto att de bidrog till mer blodlevring, något som i sin tur lockar dit ännu fler partiklar och ger en förstärkt signal.
– Uppåt 20 procent av tumörernas blodkärl sattes igen. Det räcker inte för att fungera som behandling, men man kan tänka sig att kombinera vårt system med att partiklarna dessutom har med sig ett läkemedel. Men kliniska tillämpningar ligger åtminstone tio år framåt i tiden, säger Erkki Ruoslahti.
Naomi Halas är professor i kemi vid Rice University i Houston och jagar även hon tumörer. Hon vill använda partiklar med ett skal av guldatomer som med hjälp av antikroppar hittar celler som omvandlats till tumörer. När partiklarna har fäst vid tumören höjs temperaturen i området med hjälp av infrarött ljus som passerar vävnaden utan att skada. Guldskalet på partiklarna koncentrerar värmeenergin och tumören kokas.
Guld som ändrar färg
Fredrik Höök är professor i fysik och verksam vid Nanokonsortiet i Lund. Han beskriver olika tillämpningar inom nanomedicin, varav en av de mest lovande är ny och känslig diagnostik. Den baseras på att lösningar med fria guldpartiklar kan anta olika färg.
Guldpartiklar som är kopplade till en igenkänningsmolekyl, exempelvis en antikropp, tillsätts ett prov. Då kan guldpartiklarna binda till ett ämne, exempelvis ett protein, som ökar i halt vid sjukdom. Guldpartiklarnas optiska egenskaper förändras beroende på hur mycket protein som binder till partiklarnas yta och lösningens färg avslöjar halterna bundet protein. Det behövs inte mycket av målämnet för att färgen ska skifta.
En tanke är att låta ett blodprov flöda förbi ett litet chips som mäter mängden av tusentals olika ämnen parallellt.