Emmanuelle Charpentier, 51 år, har berättat att de långa ljusa sommarnätterna i Umeå hjälpte henne i forskningen. Ofta satt hon uppe till tre på morgonen med kartläggningen av crispr/cas9. Jennifer Doudna, 56 år, ser fram emot en egen parkeringsplats, en förmån för Nobelpristagare vid Berkeley-universitetet: ”Efter 18 år kan jag äntligen parkera på campus”.
Bild: EPA / Clemens Bilan & UC Berkeley / Keegan Houser
Deras gensax revolutionerar gentekniken
Bara åtta år efter att Emmanuelle Charpentier och Jennifer Doudna presenterade sin gensax håller den på att revolutionera gentekniken. Den ger hopp om bot för svåra genetiska sjukdomar – men väcker också etiska frågor.
Jennifer Doudna berättar hur hon stod i köket och lagade middag när hon plötsligt började gapskatta.
– När min son undrade varför så svarade jag att vi upptäckt ett knasigt protein som kan hitta virus och klippa sönder dem, säger hon.
Glädje var första känslan när hon insåg betydelsen av det verktyg som hon och Emmanuelle Charpentier upptäckt, en genetisk sax som kan programmeras till att klippa av dna på ett förutbestämt ställe.
Åtta år efter artikeln i tidskriften Science där de presenterade gensaxen crispr/cas9 tar de emot Nobelpriset i kemi för metoden som gör det möjligt att ”förändra livets kod”.
Gensaxen fungerar som en ordbehandlare
Gensaxen har jämförts med en ordbehandlare på datorn. Med dess hjälp går det att ta bort, lägga till och flytta runt delar av den genetiska informationen som är lagrad i arvsmassan.
Det skapar oanade möjligheter inom en rad områden. Gensaxen används bland annat inom forskning för att kartlägga funktionen hos olika gener och hur de kan kopplas till sjukdomar. Och mängder av växter har med gensaxens hjälp fått nya egenskaper, som att stå emot torka eller insektsangrepp. Dessutom pågår intensiv forskning för att bota svåra ärftliga sjukdomar, och kliniska försök görs redan för vissa ärftliga blod- och ögonsjukdomar.
Men forskare använder även crispr på sätt som överraskat Jennifer Doudna, som att studera de färgglada mönstren på fjärilsvingar.
– Det är både förvånande och glädjande hur verktyget kan anpassas för att lösa nya problem och hitta svar på frågor jag aldrig hade kunnat drömma om, säger hon.
Väcker stora etiska frågar
Möjligheterna är enorma, men just det faktum att tekniken är så effektiv väcker samtidigt farhågor. För två år sedan, 2018, chockade den kinesiska forskaren He Jiankui världen med att han använt gensaxen för att göra två tvillingflickor resistenta mot hiv, genom att förändra deras arvsmassa redan som embryon. Men att förändra mänskliga embryon är i de flesta länder olagligt och He Jiankui dömdes senare till fängelse.
Tvillingarnas tillblivelse har gett nytt bränsle till debatten om hur genförändringar ska regleras och användas på ett ansvarsfullt sätt, en fråga som varit aktuell sedan 1970-talet.
– Diskussionen har pågått i flera decennier, men blir mer akut när vi får ett sådant här kraftfullt verktyg, säger Gunnar von Heijne, professor i teoretisk kemi och sekreterare i Nobelkommittén för kemi.
Både Emmanuelle Charpentier och Jennifer Doudna har engagerat sig i de etiska frågorna. Tillsammans med Samuel Sternberg har hon skrivit en bok i ämnet.
– Om man börjar förändra människans genetiska arv blir det svårt att förhålla sig till en gräns som inte bör överträdas. Det skulle kunna leda till transhumanism, som går ut på att förbättra människan, sa Emmanuelle Charpentier i en tidigare intervju med Forskning & Framsteg.
Forskningledare vid Umeå universitet
Emmanuelle Charpentier är född i Frankrike och i dag chef för Max Planckinstitutet för infektionsbiologi i Berlin. Men flera av de viktiga upptäckterna av gensaxens funktion gjorde hon vid Umeå universitet där hon från 2009 arbetade några år som forskningsledare.
Gensaxen grundar sig på en mekanism som bakterier använder för att försvara sig mot virus. Om bakterien överlever infektionen sparar den undan en bit av virusets dna i en särskild del av sitt eget dna, som kallas clustered regularly interspaced short palindromic repeats, crispr. Med hjälp av denna genetiska databas upptäcker och bekämpar bakterien virus genom att använda enzymet cas9 som målsökande sax, som klipper av inkräktarnas arvsmassa.
Emmanuelle Charpentier och Jennifer Doudna började samarbeta 2011 och har inte bara kartlagt den här mekanismen. De förenklade också crispr/cas9 och visade i provrörsexperiment att de kunde styra cas9 så att enzymet kapade en dna-molekyl på önskat ställe.
Utdragen patentstrid
I spekulationerna om ett Nobelpris för crispr har även Feng Zhang vid det amerikanska forskningsinstitutet Broad Institute ofta nämnts som en tredje pristagare vid sidan av Charpentier och Doudna. Han var först med att visa att gensaxen fungerar i mänskliga celler. Han är också inblandad i den utdragna patentstrid om rätten till tekniken som pågår i USA mellan Broad Institute och University of California.
Dokumentär om crispr
På Netflix finns en dokumentär om gensaxen crispr. Du ser den här.
Patentstriden visar att stora kommersiella intressen står på spel. Flera företag utvecklar nya läkemedel och behandlingar med crispr, några med pristagarna som medgrundare.
Att deras samarbetsprojekt skulle resultera i bråk om rättigheter var dock inget de kunde föreställa sig under arbetet. Liksom många andra stora vetenskapliga genombrott föddes gensaxen ur grundforskning, utan sikte på praktiska tillämpningar.
Även om gensaxen beskrivs som en ”målsökande robot” kan det uppstå oönskade fel och flera utmaningar återstår innan den kan användas i medicinska syften i människa.
– En av de största utmaningarna är att rikta en viss behandling till rätt typ av celler, säger Jennifer Doudna.
Att priset går till två kvinnor har aldrig tidigare hänt i kemiprisets historia. Med årets pristagare uppgår antalet kvinnliga kemipristagare till totalt sju.
– Jag hoppas att priset ska visa vägen för unga kvinnor till att välja en vetenskaplig karriär, säger Jennifer Doudna.
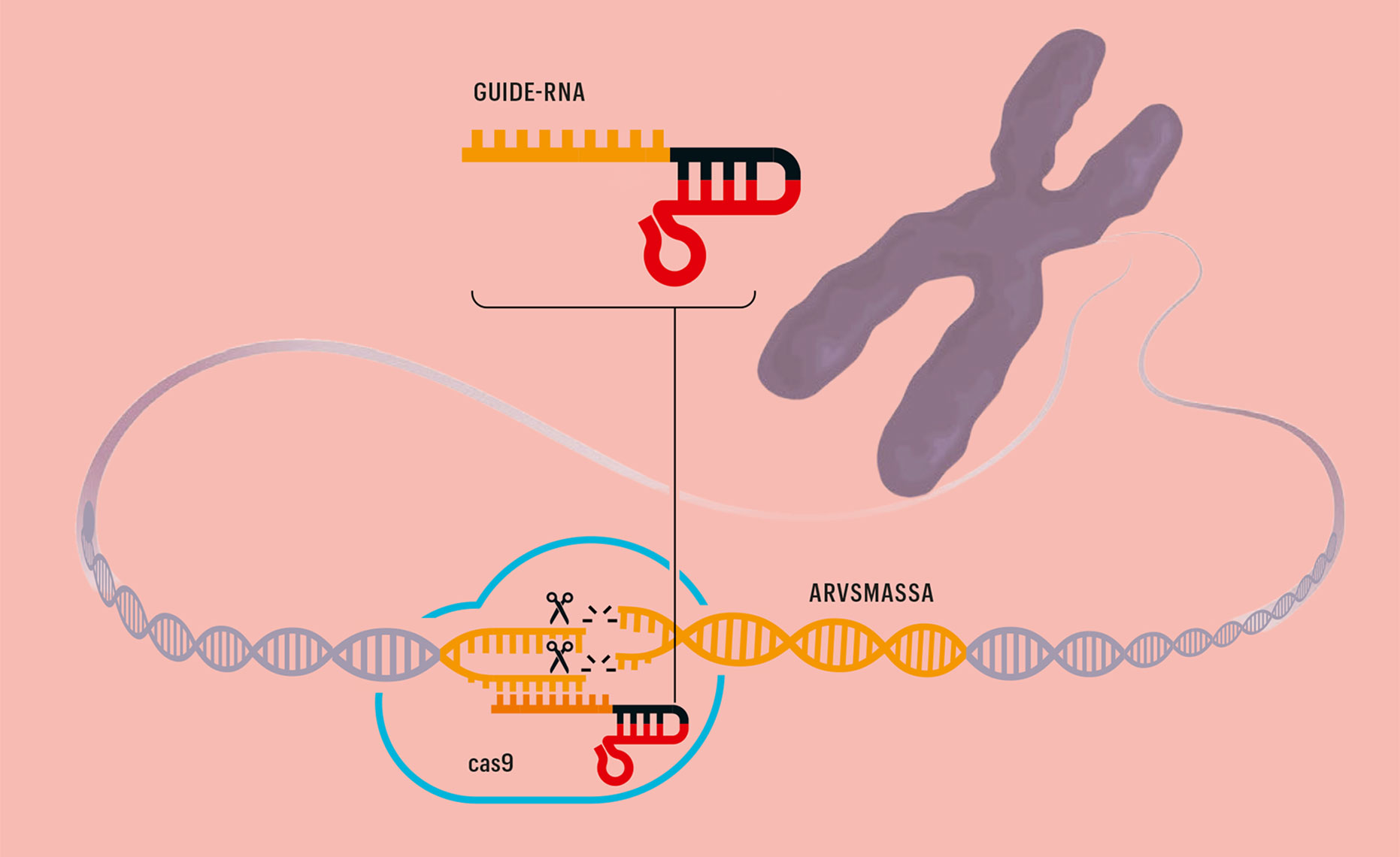
Så fungerar gensaxen
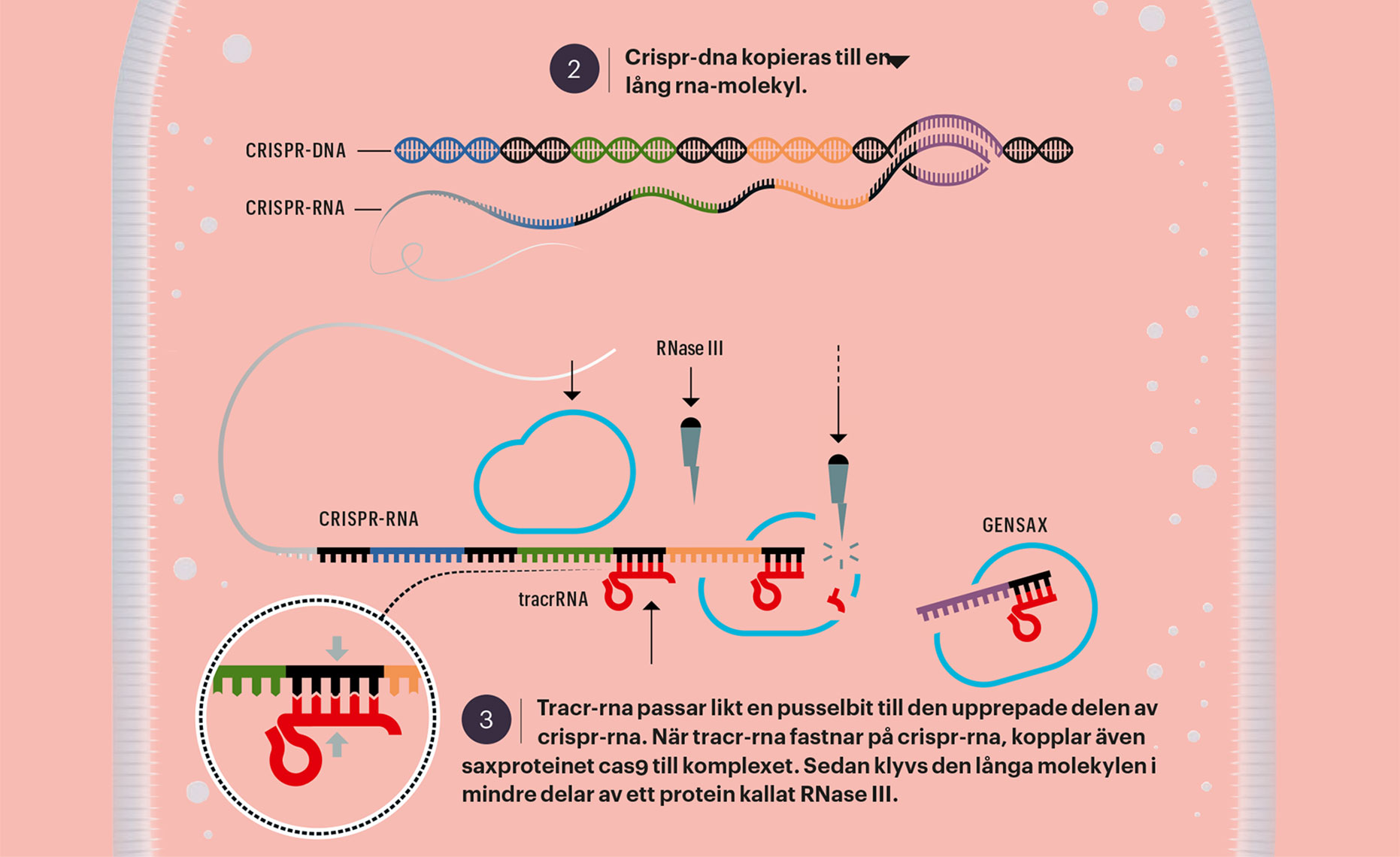
Bygger på bakteriers försvar mot virus